来源:雪球App,欧博abg作者: bioSeedin柏思荟,(https://xueqiu.com/3825493560/211576371)

Ang(血管生成素,Angiopoietin)是一种分泌型的生长因子,主要在胚胎发育期表达,与心血管系统的发育成熟关系密切。在成人体内,Ang高表达于女性生殖系统(卵巢、子宫),在其他组织中呈低水平表达。血管生成素的配体为Tie-2,二者结合后使Tie-2磷酸化,后通过激活下游通路如AKT和ERK影响血管通透性,如促进血管生成,维持血管内环境稳定,同时参与生理及病理情况下,如月经周期、脑卒中、伤口愈合、感染、肿瘤发生等的血管新生。
Ang的家族成员主要包括Ang-1、Ang-2、Ang-3和Ang-4四种因子,其中,Ang-1和Ang-2与血管生成的关系较为密切。Ang-1是由498个氨基酸组成的同源六聚体,其卷曲结构域大约有180个氨基酸。在胚胎心血管发育早期,Ang-1主要在包绕心内膜的心肌上表达,后期则在血管周细胞上表达,Ang-1的表达受缺氧、表皮生长因子(EGF)、转化生长因子-β(TGF-β)等调控。Ang-2与Ang-1存在60%的同源性,主要区别在于曲卷结构域和纤维蛋白原样结构域的交界处比Ang-1少了一个半胱氨酸。Ang-2在胚胎发育期主要表达于大血管平滑肌,在成体的子宫和胎盘等血管生成活跃的组织中表达。
Ang-1、Ang-2存在截然不同的作用机制。当Ang-1与Tie-2结合后,激活下游AKT和ERK通路,这两条通路参与减少血管生成和血管通透性,欧博官网有利于血管稳定。而Ang-2与Tie-2竞争性结合,抑制Tie-2磷酸化,从而促进血管生成。新生血管与视网膜血管性疾病的发病机制密切相关。此外,Ang/Tie2通路参与多种肿瘤的血管生成,尤其是Ang-2在肿瘤中表达水平明显升高,且可通过诱导产生内皮细胞蛋白酶、MMP-2等促进肿瘤的发展与转移。因此,通过中和Ang-2,阻止其与Tie-2结合,抑制血管生成,有望实现视网膜血管性疾病的良好控制。
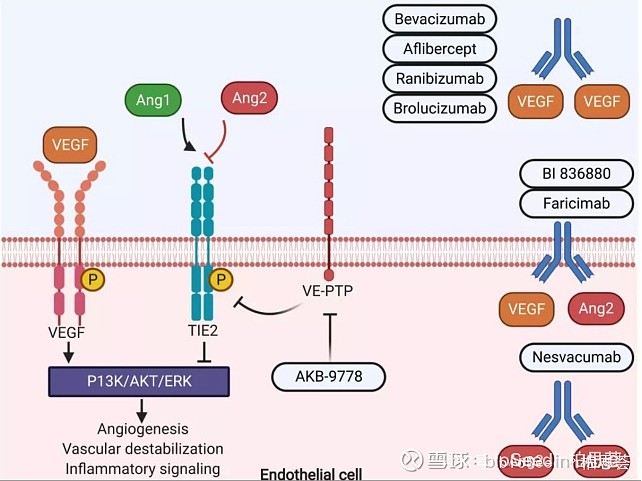
图:Ang/Tie2信号通路

目前,一批全球制药巨头纷纷布局Ang-2靶点,相关企业包括辉瑞、阿斯利康、安进、再生元、罗氏等。除了单克隆抗体外,靶向Ang-2和VEGF的双特异性抗体亦是企业重点关注的方向,有研究发现Ang-2的作用与VEGF关系密切,VEGF可增加Ang-2的表达,协同Ang-2促进血管生成,其中罗氏的Faricimab已于1月28日获FDA批准上市。
(1)单抗药物:MEDI3617是阿斯利康旗下的一款靶向Ang-2的IgG1型单克隆抗体。在2014年ASCO上,阿斯利康曾披露了MEDI3617联合化疗或贝伐珠单抗治疗实体瘤的Ⅰ期早期临床数据。但是,在2018年,CLIN CANCER RES发表了一篇文章,试验结果表明,尽管MEDI3617单药治疗卵巢癌实现6%的客观缓解率,但存在三级水肿的TRAE;此外,MEDI3617联合贝伐珠单抗治疗恶性胶质瘤未出现任何客观缓解。考虑到药物临床活性有限,阿斯利康终止了MEDI3617的研究。
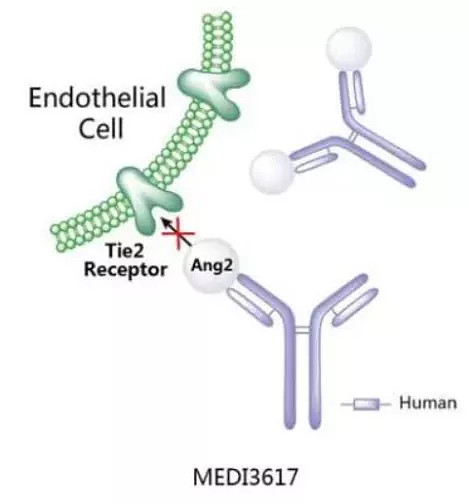
图:MEDI3617作用机制
数据来源:阿斯利康
REGN910(nesvacumab)是一款由再生元研发的靶向Ang-2的全人源单克隆抗体。2017年,拜耳与再生元达成合作,开发REGN910联合阿柏西普用于严重眼科疾病的治疗。临床前数据表明,血管生成素与血管内皮生长因子(VEGF)家族共同作用,促进了眼内血管和淋巴管的形成和成熟。因此,血管生成素2(Ang2)与VEGF共同作用有可能影响特定眼部疾病新生血管的病理学进程及血管壁的通透性。然而,在Ⅱ期临床试验中,联合给药组与阿柏西普单药组疗效并无显著性差异,因此再生元终止了REGN910的开发。
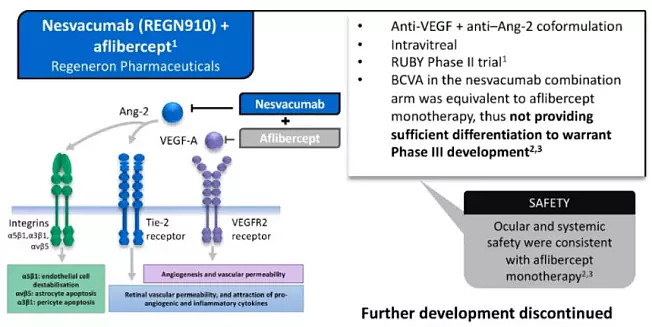
图:REGN910与阿柏西普联合疗法临床进展
数据来源:再生元
AMG780是安进研发的一款靶向Ang-1和Ang-2的IgG2型单克隆抗体,可同时阻断Ang-1和Ang-2与Tie2的结合,进而抑制肿瘤血管生成,目前正开发包括胶质母细胞瘤在内的实体瘤。在Ⅰ期临床试验中,试验纳入44名患者,共出现3例DLTs,包括1例3级血小板减少症,1例3级恶性心包积液和1例3级蛋白尿。总的来说,AMG780具有较好的耐受性,目前正处于Ⅰ/Ⅱ期临床试验。
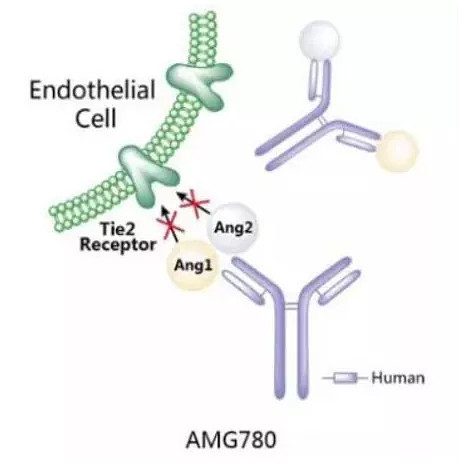
图:AMG780作用机制
数据来源:安进
(2)双抗药物:Vabysmo(Faricimab)是一款由基因泰克研发的VEGF-A/Ang-2双抗,于2022年1月28日获FDA批准上市,用于治疗湿性年龄相关性黄斑变性(wAMD)和糖尿病性黄斑水肿(DME)。Vabysmo可同时靶向Ang-2和VEGF-A两个通路,恢复血管的稳定性并减少炎症,为患有视网膜疾病的人群改善视力。
Vabysmo的临床优势主要在于较低的给药频次,临床使用为每四个月注射一次。临床试验结果表明,每四个月接受Vabysmo治疗患者的视力结果与每两个月接受阿柏西普患者视力相比,达到非劣效标准。
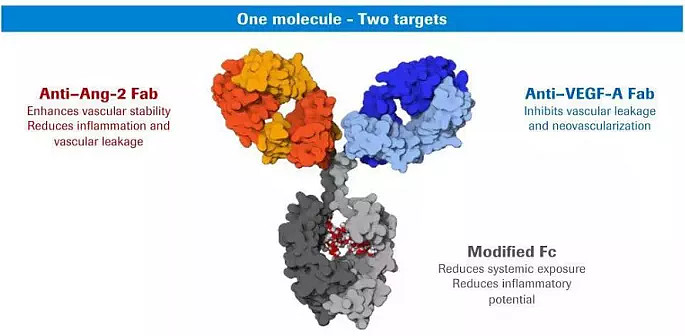
图:Vabysmo示意图
数据来源:罗氏
BI 836880是一款由勃林格殷格翰研发的具有白蛋白结合域的抗VEGF/Ang-2双特异性抗体,旨在提高wAMD患者的治疗效果。在2020年美国眼科学会年会(AAO 2020)上,勃林格殷格翰披露了BI 836880的Ⅰ期研究结果,试验包括三个剂量队列,共纳入9名患者,所有患者均接受了一次玻璃体内注射BI 836880,研究结果显示从基线到试验结束的平均BCVA变化分别为+5.3,+7.3和+0.3。安全性方面,在患者人群中未发现剂量限制事件或药物相关的严重不良事件,但存在视网膜厚度减少的问题。除了眼科疾病外,勃林格正探索BI 836880联合PD-1抑制剂Ezabenlimab(BI 754091)用于实体瘤的治疗。
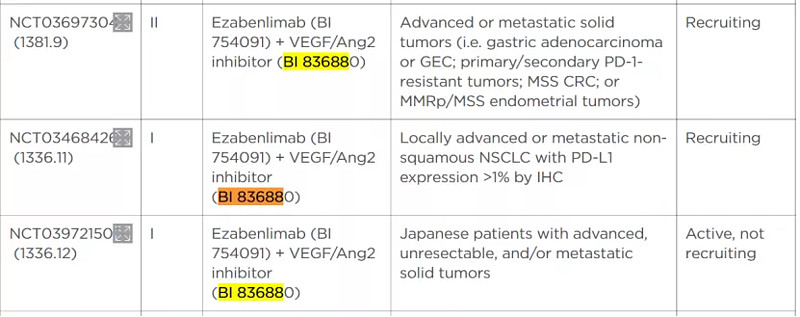
图:BI836880联合Ezabenlimab(BI 754091)治疗实体瘤
数据来源:勃林格殷格翰
血管生成素Ang是首个被确定的来源于人肿瘤组织且具有促血管生成功能的细胞因子,其家族主要包括Ang-1、2、3和4四个成员,其中,Ang-1和Ang-2与血管生成的关系较为密切。除了与肿瘤的血管生成关系密切外,Ang与视网膜血管性疾病的发病机制亦息息相关。目前,一批全球制药巨头纷纷布局Ang-2靶点,相关企业包括辉瑞、阿斯利康、安进、再生元、罗氏等。但多款靶向Ang-2的单抗遭遇临床失败,靶向Ang-2和VEGF的双特异性抗体亦或许是Ang-2靶点大放异彩的关键,罗氏的Faricimab已于1月28日获FDA批准上市,适应症包括湿性年龄相关性黄斑变性(wAMD)和糖尿病性黄斑水肿(DME)。